Comment est structuré l’atome ?
Au début du 20ième siècle l’existence de l’atome est connue, mais non sa structure. On sait seulement qu’étant électriquement neutre, il est constitué d’un mélange de corpuscules de charges négatives (électrons) et positives (plus tard baptisés protons) en nombre égal, mais on ignore tout de sa taille, de sa structure ainsi que de celle des constituants et l’on pense que ces derniers sont mélangés dans une sorte de sac (modèle humoristiquement baptisé « Plum-Pudding ») de taille inconnue.
Le seul moyen d’élucider cette structure est de « bombarder » les atomes avec des particules d’au moins d’aussi petite taille. Il faut que ces particules aient une vitesse suffisante pour émerger de la matière qu’elles percutent de manière à ce que l’on puisse observer la manière dont leur trajectoire a été perturbée.
Or au début du siècle se produit une découverte majeure : la découverte de la radioactivité par H. Becquerel et la séparation et la production d’éléments radioactifs par P. et M. Curie : le Radium et le Polonium. Ces éléments émettent des rayonnements appelés : α, β, γ.
En particulier, les particules α (alpha) sont des atomes Hélium ayant perdu leurs électrons, donc de charge positive. Elles sont de très petite taille et sont éjectées de la source radio-active avec des vitesses de l’ordre de 10 km/s, correspondant à une accélération de plusieurs millions de Volts. Avant d’être remplacées par des accélérateurs, elles vont permettre pendant environ 30 ans d’effectuer toutes sortes d’expériences de collisions qui vont résoudre complètement la structure de l’atome. F. et I. Joliot Curie découvriront également la radioactivité artificielle avec ces sources.
L’expérience de Rutherford : 3 conclusions déterminantes
E. Rutherford avait réussi à élucider la nature de ces particules α, ce pourquoi il obtient le prix Nobel en 1908. L’année suivante, il a l’intuition que par collision, elles pourront lui donner des informations sur la structure de la matière. Avec H. Geiger et E. Marsden, il envoie ainsi des particules α, sur une feuille d’or et mesure leur distribution spatiale à la sortie. L’expérience a lieu dans une chambre fermée dont l’air a été évacué afin que les particules se propagent dans le vide, sans quoi l’atmosphère aurait perturbé leurs trajectoires.
Cette expérience a mené à 3 conclusions absolument « sensationnelles » pour l’époque :
1 – « la matière est vide », car la plupart des particules passent à travers sans interaction, ce qui signifie qu’elle est concentrée dans des petits volumes.
2 – Certaines particules sont néanmoins diffusées de manière « violente », jusqu’à faire demi-tour parfois : ceci montre que les particules ont été soumises au champ des charges positives des atomes (les protons), qui les repoussent, beaucoup plus qu’aux charges négatives (électrons). Il s’ensuit que les charges négatives sont « diluées » et qu’il existe au centre des atomes un « noyau » extrêmement petit et de charge exclusivement positive.
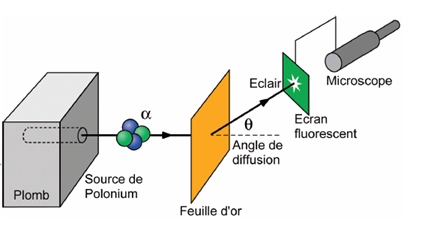
Schéma de l’expérience de Geiger, Marsden et Rutherford
3 – Le fait que les électrons ne sont pas mélangés avec les protons et sont situés à des distances de ce noyau beaucoup plus grandes que sa taille est une surprise. E. Rutherford y réfléchira pendant 2 ans avant de proposer ce modèle ! Il faudra de nombreuses années pour que cette structure soit admise et comprise par la communauté scientifique. En effet, en mécanique classique, seule connue à cette époque, les électrons devraient tourner autour du noyau, rayonner de l’énergie électromagnétique et finir par « tomber » sur le noyau aboutissant ainsi à une contradiction complète avec les observations de l’expérience. Cette contradiction va obliger à considérer les particules comme des ondes et contribuer à fonder la mécanique quantique, ce qui va demander une quinzaine d’années supplémentaires (équation de Schrödinger, 1925).
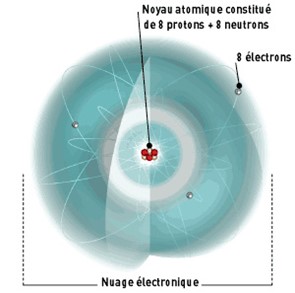
Représentation artistique de l’atome d’Oxygène avec son cortège d’électrons qui occupent l’espace à la manière d’un nuage diffus. Ce nuage a une taille environ 105 fois et, donc, un volume 1015 fois plus grand celui du noyau !
Des premières expériences de collisions aux accélérateurs de particules
Cette expérience peut être considérée comme l’ancêtre et l’archétype de toutes celles qui ont suivi. On y remarque la plupart des éléments des expériences de collisions :
- un faisceau issu d’une source
- un accélérateur (confondu avec la source ici)
- des chambres à vide pour que les particules puissent se propager
- un espace de glissement et de préparation du faisceau (iris non montré ici, focalisation par la suite)
- une cible (feuille d’or)
- un détecteur (scintillateur + microscope)
Afin d’explorer des détails de plus en plus fins de la structure de la matière, tels la structure du noyau, il faut disposer de faisceaux de particules beaucoup plus intenses et d’énergies de plus en plus élevées (jusqu’à 1 million de fois celle des particules alpha au LHC au CERN à Genève). Ceci a entrainé la construction d’accélérateurs à partir des années 1930. Ces derniers ont évolué vers des machines de plus en plus diversifiées, dont ACO constitue une des étapes dans leur histoire.


Accélérateur électrostatique inventé par E. Walton et J. Cockroft (de part et d’autre d’E. Rutherford sur la photo)
ACO appartient à une génération de machines qui réalisent des collisions faisceau-faisceau plutôt que sur cible fixe, l’anneau de stockage, rempli par un premier accélérateur, permettant d’atteindre de fortes intensités. Par la suite, il a servi de source de rayonnement synchrotron appliquée à de tous autres usages.
Mais ceci est une autre histoire !